.New insight into how plant cells divide
http://blog.naver.com/mssoms
http://jl0620.blogspot.com
http://jk0620.tripod.com
https://www.facebook.com/junggoo.lee.9
.New insight into how plant cells divide
식물 세포가 어떻게 분열하는지에 대한 새로운 통찰력
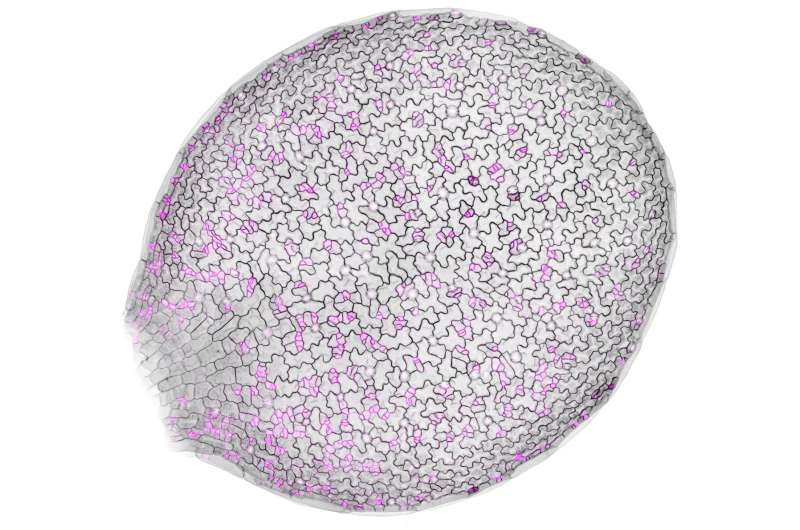
Elise Overgaard, 스탠포드 대학 세포 경계(검은색)와 극성 단백질(자홍색)을 표시하는 형광 단백질을 발현하도록 변형된 애기장대 식물의 발달 중인 잎입니다. 이 기술을 통해 저자는 살아있는 식물의 줄기 세포 내에서 단백질 역학을 연구할 수 있었습니다. 크레딧: Andrew Muroyama JULY 6, 2023
-줄기 세포가 분열할 때마다 하나의 딸 세포는 줄기 세포로 남고 다른 하나는 자체 발달 여정을 떠납니다. 그러나 두 딸 세포는 운명을 완수하기 위해 특정하고 다른 세포 물질이 필요합니다. 동물 줄기 세포는 분열하는 동안 부모 세포에서 각 딸 세포로 정확한 물질을 물리적으로 끌어오기 위해 구조적 세관의 일시적인 네트워크인 세포골격을 사용합니다.
식물은 또한 각각의 딸에게 다른 물질을 분배해야 하는 줄기 세포를 가지고 있지만 이전 연구에서는 이 작업을 수행하기 위해 "동물 스타일" 세포 골격을 배제한 것으로 보입니다. 그리고 대신에 어떤 식물을 사용했는지는 지금까지 파악하기 어려웠습니다. 7월 6일 사이언스 에 발표된 새로운 연구에서 스탠포드 대학의 연구원들은 식물 세포 도 세포골격을 사용한다는 사실을 발견했습니다. 하지만 반전이 있습니다. 그들이 연구한 식물 세포는 동물 줄기세포처럼 세포골격을 당기는 대신 실제로 밀어냈습니다.
-"세포골격을 사용하여 '이쪽으로 나누어!'라고 말하는 대신에 식물 은 '이대로 나누지 마세요!'라고 말했습니다. " 전 Stanford에서 박사 후 과정 연구원이자 현재 University of California, San Diego의 조교수이자 논문의 주저자인 Andrew Muroyama가 말했습니다. 새로운 발견은 연구원들이 변화하는 환경에 더 잘 적응할 수 있는 식물을 설계하는 데 도움이 될 수 있습니다. 이는 세계가 기후 변화에 계속 직면함에 따라 중요한 과제입니다.
"줄기 세포가 동물에서 어떻게 분열하는지 이해하는 것은 다양한 인간 질병을 이해하는 데 중요했으며 중개 의학에 영향을 미쳤습니다."라고 Muroyama는 말했습니다. "저는 줄기 세포가 식물에서 어떻게 분열하는지에 대한 우리의 이해를 개선하면 미래의 공학 응용 분야에 정보를 제공할 수 있다는 유사한 희망을 가지고 있습니다."
재앙을 위협하여 벽 건설을 막음
Dominique Bergmann, Shirley R. 및 Leonard W. Ely, Jr. 교수의 생물학 교수는 각 세포에서 중요한 단백질의 작은 클러스터인 극성 복합체를 조사하여 이 작업을 시작했습니다. 적절한 크기와 모양의 잎을 만들기 위해. 극성 복합체는 분열하는 잎 줄기 세포가 스스로 방향을 잡도록 도와줍니다. "줄기 세포는 분열할 위치를 결정하기 위해 이러한 극성 단백질을 사용합니다."라고 Muroyama는 말했습니다.
"우리는 그 단백질들이 분열에 관여한다는 것을 알고 있었지만, 그들이 분자 수준에서 그 과정을 어떻게 통제하는지 몰랐습니다." 이 단백질이 어떻게 작용하는지 조사하기 위해 연구팀은 극성 복합체와 세포골격 단백질의 형광 버전을 발현하는 식물 세포주를 개발한 다음 암실에서 수백 시간 동안 세포가 성장하고 분열하고 반복되는 동안 빛나는 단백질의 움직임을 추적했습니다.
https://scx2.b-cdn.net/gfx/video/2023/new-insight-into-how-p.mp4
극성 단백질, BASL(자홍색) 및 미세소관(검은색) 사이의 상호작용. 미세소관이 분극화된 영역으로 성장할 수 있지만 빠르게 수축하여 식물 세포 내에 미세소관이 고갈된 영역을 생성하는 방법에 유의하십시오. 크레딧: Andrew Muroyama
-그들은 곧 일부 세포가 일반적으로 식물 세포 분열을 지배하는 "가장 짧은 벽 규칙"에 따라 분열하지 않는다는 것을 관찰했습니다. 식물 세포는 세포를 분할할 수 있는 가장 작은(따라서 가장 에너지적으로 보존적인) 벽을 만들 것으로 예상되지만, 어떤 경우에는 극성 복합체가 그 벽을 만들어야 할 바로 그 위치에 있었습니다. 어쨌든 그것은 건설을 막았습니다. 일련의 엄격한 실험을 통해 연구원들은 극성 복합체가 벽의 구성을 가능하게 하는 미세소관을 밀어내고 있다는 결론을 내렸습니다.
"극성 콤플렉스는 '미세소관 중 누군가가 내 영역을 잠식하려고 하면 강제로 쫓아내겠다. 나는 말 그대로 대재앙을 일으킬 것이다. 이는 미세소관을 완전히 파괴하는 기술 용어다. 그래서 당신은 할 수 있다.' 이 구역을 침범하지 마십시오'라고 Bergmann이 말했습니다. 변화하는 기후에 대한 관리 Bergmann의 연구실은 식물이 변화하는 환경에 대처하는 방식인 탄력성에 관심이 있습니다.
-식물은 잎이나 가지 패턴, 또는 호흡하거나 당을 저장하는 속도를 변경하여 생존합니다. "이 연구는 예를 들어 식물 구조를 변경하거나 식물이 변화하는 기후에 적응하도록 돕기 위해 줄기 세포 행동을 조정할 수 있는 응용 프로그램으로 이어질 수 있습니다."라고 Muroyama는 말했습니다. 환경의 신호에 어떻게 반응할지에 대한 결정은 줄기 세포 에 의해 지시됩니다 .
이 과정에서 Bergmann은 극성 복합체를 구성 관리자와 비교하여 줄기 세포가 제대로 분할되도록 하는 방향을 제시합니다. "이 건설 관리자는 환경으로부터 신호를 받고 무엇을 할지 결정하고 셀에 '예, 분할해야 합니다.'라고 말합니다. 그러나 그것은 또한 '이제 당신은 헤어졌습니다. 가서 당신의 행운을 찾으십시오'라고 말합니다."라고 Bergmann은 말했습니다.
이제 연구원들은 이 관리자가 어떻게 작동하는지 알았으므로 업스트림 및 다운스트림 프로세스에서 관리자의 역할을 결정하고 그 힘을 활용하는 방법을 알아낼 수 있습니다. "정확히 극성 복합체가 작동하는 방식은 우리가 여전히 알아내야 할 부분입니다."라고 Bergmann은 말했습니다.
"정말 멋진 특수 세포, 즉 흥미로운 모양을 만드는 세포, 흥미로운 화학 물질을 만드는 세포, 특정 자극에 반응하는 세포를 만드는 이 모든 식물을 어떻게 얻을 수 있을까요? 그리고 그렇게 되도록 설계할 수 있을까요?"
추가 정보: Andrew Muroyama 외, Cortical polarity는 기공 혈통에서 고유한 비대칭 상속을 보장하여 잎 표면을 패턴화합니다, Science (2023). DOI: 10.1126/science.add6162 저널 정보: 과학 스탠퍼드대 제공
https://phys.org/news/2023-07-insight-cells.html
==================================
메모 2307071043 나의 사고실험 oms 스토리텔링
식물의 잎사귀나 동물의 피부가 내부와 외부를 나뉘는 경계 세포가 존재하는 것으로 그 기능에 차이가 드러났다. 줄기세포가 증식하여 샘플링 oms.full을 가지는데 빈공간이 필요한 모양이다. 그것이 경계 빈(0)세포이다. 두께가 내부(inside_cell)와 외곽(outside_cell)에 다르게 존재할 수 있다. 특히 외곽의 두께는 outside_cell.abs=|1|은 oms=1을 함의 할 수 있는 영역이다.
이들 생물학적 경계세포 영역이 중요한 이유는 샘플링 oss.base에서 banc.oms_dimension (n*oms.hypercube)확장으로 야기된 시공간이 존재하는데, 이곳이 내부와 외부를 통하는 미세소관 경로를 함의한다. 허허.

-They soon observed that some cells do not divide according to the "shortest wall rule" that normally governs plant cell division. Plant cells would be expected to build the smallest (and therefore most energetically conserved) walls that could divide the cell, but in some cases the polar complex was just there to build that wall. Somehow it prevented construction. Through a series of rigorous experiments, the researchers concluded that the polar complex was pushing away the microtubules that made the construction of the wall possible.
==================================
memo 2307071043 my thought experiment oms storytelling
The difference in function was revealed by the existence of border cells that divide the inside and outside of the leaves of plants and the skin of animals. Stem cells proliferate and have sampling oms.full, but it seems that empty space is needed. That is the border empty (0) cell. Different thicknesses may exist in the inside (inside_cell) and outside (outside_cell). In particular, outside_cell.abs=|1| for the outer thickness is an area that can imply oms=1.
The reason why these biological boundary cell regions are important is that there is a space-time caused by the banc.oms_dimension (n*oms.hypercube) expansion in the sampling oss.base, which implies the microtubule pathway through the inside and outside. haha.
Samplea.oms (standard)
b0acfd 0000e0
000ac0 f00bde
0c0fab 000e0d
e00d0c 0b0fa0
f000e0 b0dac0
d0f000 cae0b0
0b000f 0ead0c
0deb00 ac000f
ced0ba 00f000
a0b00e 0dc0f0
0ace00 df000b
0f00d0 e0bc0a
sampleb. qoms (standard)
0000000011=2,0
0000001100
0000001100
0000010010
0001100000
0101000000
0010010000
0100100000
2000000000
0010000001
sample b.poms (standard)
q0000000000
00q00000000
0000q000000
000000q0000
00000000q00
0000000000q
0q000000000
000q0000000
00000q00000
0000000q000
000000000q0
Samplec.oss (standard)
zxdxybzyz
zxdzxezxz
xxbyyxzz
zybzzfxzy
cadccbcdc
cdbdcbdbb
xzezxdyyx
zxezybzyy
bddbcbdca

.Profound Paradigm Shift in Cellular Biology – DNA Damage Repaired by Antioxidant Enzymes
세포 생물학의 심오한 패러다임 변화 – 항산화 효소에 의해 복구되는 DNA 손상

주제:암유전학분자 생물학 작성자: 게놈 규제 센터 2023년 7월 6일 DNA 손상 개념 그림
연구원들은 세포의 핵이 손상 시 DNA 무결성을 보호하기 위해 이동하는 세포 효소와 함께 대사적으로 활성화된다는 사실을 발견했습니다. 세포 대사에 대한 이러한 이해의 변화는 암 세포가 종종 성장을 위해 대사 과정을 가로채기 때문에 암 치료의 새로운 전략을 알릴 수 있습니다. 위기 상황에서 핵은 항산화 효소를 불러 구조합니다.
신진대사적으로 활성화되는 핵은 암 연구에 영향을 미치는 심오한 패러다임 전환입니다. 바르셀로나의 CRG와 비엔나의 CeMM/의과 대학의 연구원들이 분자 시스템 생물학(Molecular Systems Biology) 에 발표한 새로운 연구 결과에 따르면 인간의 핵은 대사적으로 활성화되어 있습니다 . 광범위한 DNA 손상 과 같은 위기 상황에서 핵은 게놈의 무결성을 위협하는 긴급 수리를 수행하기 위해 미토콘드리아 기계를 사용하여 스스로를 보호합니다.
핵은 역사적으로 세포질의 공급망을 통해 필요한 모든 것을 가져오면서 대사적으로 불활성인 것으로 여겨졌기 때문에 이번 발견은 패러다임 전환을 나타냅니다. 암은 자유로운 성장을 위해 세포 대사를 가로채고 있습니다. 이 발견은 약물 내성을 극복하고 궁극적으로 새로운 치료법을 설계할 수 있는 새로운 단서를 제공함으로써 암 연구의 미래 방향을 안내하는 데 도움이 될 수 있습니다.

PRDX1의 DNA 손상 Colocalization 이미지는 DNA 손상 위치(이 4개 세포의 핵에서 - 녹색)와 PRDX1의 공동 국소화(빨간색, 같은 위치)를 보여줍니다. 크레딧: 사라 Sdelci / CRG 전형적인 인간 세포는 대사적으로 활동적이며, 영양소를 에너지로 변환하는 화학 반응과 생명을 유지하는 유용한 제품으로 포효합니다. 이러한 반응은 또한 산소와 물이 금속을 부식시키고 녹을 형성하는 것과 같은 방식으로 DNA의 구성 요소를 손상시키는 과산화수소와 같은 위험한 부산물인 활성 산소 종을 생성합니다.
녹의 누적 효과로 인해 건물이 무너지는 것처럼 활성 산소 종은 게놈의 무결성을 위협합니다. 세포는 핵 외부와 세포질 및 미토콘드리아 내에서 대사 활동을 포함함으로써 에너지 요구 사항의 균형을 섬세하게 유지하고 DNA 손상을 방지하는 것으로 생각됩니다.
항산화 효소는 약 30억 개의 뉴클레오티드가 잠재적으로 치명적인 돌연변이를 겪지 않도록 보호하는 방어 전략인 DNA에 도달하기 전에 소스에서 활성 산소 종을 제거하기 위해 배치됩니다. 어쨌든 DNA 손상이 발생하면 세포는 잠시 멈추고 수리를 수행하여 새로운 빌딩 블록을 합성하고 틈을 채웁니다. 게놈 무결성을 유지하는 데 있어서 세포 대사의 중심적인 역할에도 불구하고 대사 교란이 DNA 손상 및 복구 과정에 어떤 영향을 미치는지에 대한 체계적이고 편견 없는 연구는 없었습니다.
이것은 자유로운 성장을 위해 대사 과정을 가로채는 능력을 특징으로 하는 암과 같은 질병에 특히 중요합니다.

Sara Sdelci 연구소 그룹 사진 바르셀로나의 게놈 규제 센터 구내에서 Dr. Sara Sdelci가 이끄는 그룹의 사진. 신용: CRG
바르셀로나에 있는 CRG(Centre for Genomic Regulation)의 사라 스델시(Sara Sdelci)와 빈에 있는 오스트리아 과학 아카데미 분자 의학을 위한 CeMM 연구 센터의 조안나 로이조우(Joanna Loizou)가 이끄는 연구팀과 비엔나 의과대학은 다양한 연구를 수행하여 이 문제를 해결했습니다. 어떤 대사 효소와 과정이 세포의 DNA 손상 반응에 필수적인지 확인하기 위한 실험. 연구 결과는 Molecular Systems Biology 저널에 오늘 발표되었습니다. 연구자들은 에토포사이드(etoposide)로 알려진 일반적인 화학 요법 약물을 사용하여 인간 세포주에서 실험적으로 DNA 손상을 유도했습니다.
Etoposide는 DNA 가닥을 끊고 손상을 복구하는 데 도움이 되는 효소를 차단함으로써 작동합니다. 놀랍게도 DNA 손상을 유도하면 활성 산소종이 생성되어 핵 내부에 축적됩니다. 연구자들은 활성 산소 종의 주요 공급원인 세포 호흡 효소가 DNA 손상에 반응하여 미토콘드리아에서 핵으로 재배치되는 것을 관찰했습니다. 이 발견은 핵이 대사적으로 활동적임을 암시하기 때문에 세포 생물학의 패러다임 전환을 나타냅니다.
“연기가 있는 곳에 불이 있고 활성 산소가 있는 곳에 대사 효소가 작용합니다. 역사적으로 우리는 핵을 세포질에서 필요한 모든 것을 가져오는 대사적으로 불활성인 소기관으로 생각했지만, 우리의 연구는 또 다른 유형의 대사가 세포에 존재하고 핵에서 발견된다는 것을 보여줍니다.”라고 Sara Sdelci 박사는 말합니다. 연구 저자이자 게놈 규제 센터의 그룹 리더입니다. 연구원들은 또한 CRISPR-Cas9를 사용하여 이 시나리오에서 세포 생존에 중요한 모든 대사 유전자를 식별했습니다.
이 실험을 통해 세포는 미토콘드리아에서 일반적으로 발견되는 항산화 효소인 PRDX1 효소가 핵으로 이동하여 더 이상의 손상을 방지하기 위해 존재하는 활성 산소 종을 제거하도록 지시한다는 사실이 밝혀졌습니다. PRDX1은 또한 DNA의 빌딩 블록인 뉴클레오타이드 합성에 중요한 원료인 아스파테이트의 세포 가용성을 조절하여 손상을 복구하는 것으로 밝혀졌습니다. “PRDX1은 로봇 수영장 청소기와 같습니다. 세포는 내부를 "깨끗하게" 유지하고 활성 산소 종의 축적을 방지하기 위해 그것을 사용하는 것으로 알려져 있지만 이전에는 핵 수준에서 사용하지 않았습니다. 이것은 위기 상황에서 핵이 미토콘드리아 기계를 전유함으로써 반응하고 긴급한 급속한 산업화 정책을 수립한다는 증거입니다.”라고 Sdelci 박사는 말합니다.
이 발견은 미래의 암 연구 방향을 안내할 수 있습니다. 이 연구에 사용된 에토포사이드와 같은 일부 항암제는 DNA를 손상시키고 복구 과정을 억제하여 종양 세포를 죽입니다. 충분한 손상이 축적되면 암세포는 자동 파괴되는 과정을 시작합니다. 실험 중에 연구자들은 세포 호흡(산소와 영양소로부터 에너지를 생성하는 과정)에 중요한 대사 유전자를 제거하면 정상적인 건강한 세포가 에토포사이드에 저항성을 갖게 된다는 사실을 발견했습니다. 많은 암 세포가 해당 작용을 하기 때문에 이번 발견은 중요합니다. 즉, 산소가 있는 상태에서도 세포 호흡을 하지 않고 에너지를 생성한다는 의미입니다.
이것은 에토포사이드 및 유사한 메커니즘을 가진 다른 화학 요법이 해당 종양 치료에 제한된 효과를 가질 가능성이 있음을 의미합니다. 이 연구의 저자는 약물 내성을 극복하고 암세포를 더 빨리 죽이기 위해 활성 산소 종의 생성을 촉진하는 약물과 에토포사이드를 결합한 이중 치료법과 같은 새로운 전략의 탐구를 요구합니다. 그들은 또한 에토포사이드를 뉴클레오티드 합성 과정의 억제제와 결합하면 DNA 손상의 복구를 막고 암세포가 올바르게 자폭하도록 함으로써 약물의 효과를 강화할 수 있다고 가정합니다.
교신저자이자 분자의학센터 및 비엔나 의과대학의 그룹 리더인 Dr. Joanna Loizou는 새로운 생물학적 과정을 발견하기 위해 데이터 기반 접근 방식을 취하는 것의 가치를 강조합니다. “CRISPR-Cas9 스크리닝 및 대사체학과 같은 공정한 기술을 사용함으로써 우리는 DNA 복구 및 대사라는 두 가지 기본적인 세포 과정이 어떻게 얽혀 있는지 알게 되었습니다. 우리의 연구 결과는 암에서 이 두 가지 경로를 표적으로 삼는 것이 환자의 치료 결과를 어떻게 향상시킬 수 있는지에 대해 밝혔습니다.”
참조: Amandine Moretton, Savvas Kourtis, Antoni Ganez Zapater, Chiara Calabrò, Maria Lorena Espinar Calvo, Frederic Fontaine, Evangelia Darai, Etna 작성 2023년 6월 1일 , 분자 시스템 생물학 DOI: 10.15252/msb.202211267
댓글